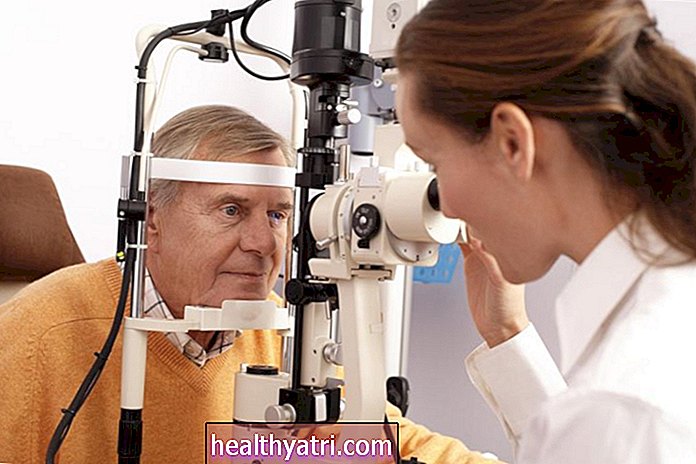
على الرغم من أن التدخين لا يزال السبب الرئيسي لسرطان الرئة ، فهو مسؤول عن 80٪ إلى 90٪ من جميع حالات سرطان الرئة ، إلا أن الوراثة قد تساهم في الإصابة بسرطان الرئة في بعض الحالات. وتشير التقديرات إلى أن 8٪ من سرطانات الرئة مرتبطة بسرطان الرئة. الاستعداد: قد يزداد خطر الإصابة بسرطان الرئة إذا كان أحد الوالدين أو الأشقاء مصابًا بالمرض ؛ ومع ذلك ، فهذا لا يعني أنك ستصاب بالتأكيد بالمرض إذا أصيب به شخص آخر في عائلتك.
تشير مجموعة الأبحاث الحالية إلى أن الجينات من المرجح أن تساهم في الإصابة بسرطان الرئة لمن هم:
- يونغ (تحت سن 50)
- أنثى
- لم يدخنوا أبدًا
حدد العلماء بعض الطفرات الجينية (التغيرات في الشفرة الجينية الخاصة بك) التي قد تزيد من خطر الإصابة بسرطان الرئة. لكن هذا لا يعني أن جميع الطفرات الجينية المرتبطة بسرطان الرئة موروثة. يمكنك أن ترث الطفرات الجينية ، أو يمكنك اكتساب هذه التغييرات في أي وقت خلال حياتك بسبب عوامل بيئية (مثل التدخين أو التلوث).
رسم توضيحي بواسطة JR Bee ، Verywell
العوامل المؤثرة
لا يمكن للتاريخ العائلي وحده أن يتنبأ بما إذا كنت ستصاب بسرطان الرئة أم لا. سرطان الرئة العائلي هو مصطلح قد يشير إلى أن جين السرطان "ينتقل" من الآباء إلى الأبناء.
اليوم ، يعتبر الباحثون سرطان الرئة العائلي بمثابة عيارمزيجالعوامل الوراثية والبيئية التي تزيد من خطر الإصابة بسرطان الرئة بين أفراد الأسرة.
بشكل عام ، الأفراد الذين لديهم قريب من الدرجة الأولى (والد ، أو شقيق ، أو طفل) مصاب بسرطان الرئة يزيد لديهم خطر الإصابة بالمرض بمقدار 1.5 مرة تقريبًا مقارنة بأولئك الذين ليس لديهم تاريخ عائلي. هذا صحيح لكل من المدخنين وغير المدخنين.
غالبًا ما يساهم تاريخ التدخين بشكل جوهري في خطر الإصابة بسرطان الرئة أكثر من الاستعداد الوراثي للمرض.
تشير الأدلة الحالية إلى أن الخطر العائلي للإصابة بسرطان الرئة يتأثر بعدة عوامل متقاطعة ، بما في ذلك:
- الوراثة
- أنماط حياة مماثلة (مثل التدخين والنظام الغذائي)
- بيئات مماثلة (مثل تلوث الهواء الداخلي والخارجي)
التدخين السلبي داخل المنزل ، على سبيل المثال ، يمكن أن يزيد من خطر إصابة الشخص بسرطان الرئة بنسبة 20٪ إلى 30٪. وبالمثل ، فإن التعرض للرادون في المنزل - وهو السبب الرئيسي الثاني لسرطان الرئة في الولايات المتحدة - قد يؤدي أيضًا إلى الخطر العائلي للإصابة بالمرض.
على هذا النحو ، لا يمكن للتاريخ العائلي للإصابة بسرطان الرئة أن يتنبأ كثيرًا باحتمالية الإصابة بالمرض ، حيث يبرز الحاجة إلى ضبط عوامل الخطر القابلة للتعديل والحفاظ على حالة تأهب قصوى لأي علامات أو أعراض لسرطان الرئة.
دليل على المخاطر الجينية
هناك عدد من العوامل التي تشير إلى وجود عنصر وراثي صغير عندما يتعلق الأمر بخطر الإصابة بسرطان الرئة.
أصغر سنا
في الولايات المتحدة ، يبلغ متوسط العمر الذي يتم فيه تشخيص سرطان الرئة 70. ومع ذلك ، هناك أشخاص تم تشخيص إصابتهم بسرطان الرئة قبل ذلك بفترة طويلة. في الواقع ، تحدث حوالي 1.3٪ من جميع حالات سرطان الرئة لدى الأشخاص الذين تقل أعمارهم عن 35 عامًا.
الأمر المثير للاهتمام حول هؤلاء الشباب هو أن القليل منهم مدخنون ، مما يثير تساؤلات حول العوامل الأخرى التي قد تساهم في الخطر. الأشخاص الذين يصابون بسرطان الرئة في سن أصغر هم أكثر عرضة للتغييرات الجينية المرتبطة بالمرض.
لكن لم يتم إثبات ارتباط وراثي لهذه التغيرات الجينية.
جميع سرطانات الرئة تقريبًا لدى الشباب هي سرطانات غدية ، وهي نوع من السرطان يرتبط ارتباطًا وثيقًا ببعض الطفرات الجينية المكتسبة (غير الوراثية).
الجنس
يتساوى احتمال إصابة الرجال والنساء بسرطان الرئة. لا تزال هناك فوارق بين الجنسين.
لا تكون النساء أكثر عرضة للإصابة بسرطان الرئة في سن مبكرة أكثر من الرجال فحسب ، ولكنهن أيضًا أكثر عرضة للإصابة به من نظرائهن من الرجال الذين لديهم نفس عوامل الخطر.
وفقًا لمراجعة 2019 فيأبحاث سرطان الرئة متعدية ،النساء اللائي لديهن 40 عبوة من التدخين معرضات لخطر الإصابة بسرطان الرئة بمقدار ثلاثة أضعاف مقارنة بالرجال الذين لديهم نفس سجل التدخين.
قد تلعب العوامل الوراثية أو الهرمونية دورًا ، ربما عن طريق زيادة قابلية المرأة البيولوجية للإصابة بالمسرطنات (العوامل المسببة للسرطان) في دخان التبغ.
وجدت العديد من الدراسات أن النساء لديهن تركيزات أعلى من إنزيم يسمى CYP1A1 ، والذي يمكن أن يخفف من استجابة الجسم للمواد المسرطنة في الرئتين ويعزز تطور السرطان. ترتبط بعض الأشكال الجينية (الاختلافات) بخلل في تنظيم إنتاج CYP1A1 وقد تفسر سبب كون النساء أكثر عرضة لاستنشاق المواد المسرطنة.
العنصر
العرق والعرق هي أيضا عوامل مختلفة في خطر الإصابة بسرطان الرئة. تشير البيانات المستمدة من برنامج المراقبة وعلم الأوبئة والنتائج النهائية (SEER) المستمر إلى أن الأمريكيين الأفارقة معرضون لخطر الإصابة بسرطان الرئة أكبر بكثير من أي مجموعة عرقية أو عرقية أخرى.
قدمت بيانات SEER معدلات الإصابة بسرطان الرئة لمجموعات مختلفة (موصوفة في عدد الحالات لكل 100.000 شخص):
- السود: 76.1 لكل 100،000
- البيض: 69.7 لكل 100،000
- الهنود الحمر: 48.4 لكل 100.000
- سكان جزر آسيا / المحيط الهادئ: 38.4 لكل 100،000
- ذوي الأصول الأسبانية: 37.3 لكل 100.000
على الرغم من أن أشياء مثل التدخين والبيئة تساهم بالتأكيد في هذه المعدلات ، فقد لاحظ العلماء أيضًا أن الطفرات الجينية المرتبطة بسرطان الرئة يمكن أن تختلف أيضًا حسب العرق.
قد تحدد الدراسات المستقبلية مدى أهمية هذه الطفرات في المساهمة في المخاطر بين الأعراق والأعراق المختلفة ، وما إذا كانت الطفرات الجينية موروثة أو مكتسبة.
الطفرات الجينية
ترتبط بعض أنواع سرطان الرئة ارتباطًا وثيقًا بطفرات جينية محددة أكثر من غيرها ، ولكن لم يتم إثبات أنها موروثة. في الواقع ، يُعتقد أنه تم الحصول عليها. يمكن أن تغير هذه الطفرات وظيفة الخلية ودورة حياتها ، مما يؤدي إلى تكاثرها بشكل غير طبيعي وخارج نطاق السيطرة ، مما يؤدي إلى ظهور السرطان.
حدد العلماء بعض الطفرات الجينية المرتبطة بالتسرطن (تطور السرطان) في الرئتين. ترتبط الغالبية العظمى من هذه الطفرات بسرطانات الرئة ذات الخلايا غير الصغيرة (NSCLC) ، وخاصة سرطان الرئة الغدي ، على عكس سرطانات الرئة ذات الخلايا الصغيرة (SCLC).
لا يعني وجود طفرة جينية مرتبطة بسرطان الرئة أنك ستصاب بسرطان الرئة. على عكس طفرات BRCA المستخدمة للتنبؤ باحتمالية الإصابة بسرطان الثدي لدى الأفراد المعرضين لخطر كبير ، لا توجد طفرة جينية أو اختبار يمكنه التنبؤاحتماليةلسرطان الرئة.
EGFR
يمكن لطفرات جين EGFR أن تغير إنتاج بروتين يسمى مستقبل عامل نمو البشرة الذي يساعد الخلايا على الاستجابة بشكل مناسب لبيئتها. لا يوجد ما لا يقل عن 10 طفرات EGFR معروفة بأنها مرتبطة بسرطان الرئة ؛ ومن المتوقع تحديد المزيد.
تشير الأبحاث إلى أن 47٪ من الآسيويين المصابين بـ NSCLC لديهم طفرة EGFR. حوالي 21 ٪ من الأشخاص الذين يعانون من NSCLC المنحدرين من أصل شرق أوسطي أو أفريقي يحملون أيضًا الطفرة ؛ وينطبق الشيء نفسه على 12٪ من المرضى من أصل أوروبي.
تعد طفرات EGFR أكثر شيوعًا عند النساء وغير المدخنين. بينما ترتبط طفرات EGFR بشكل أساسي بسرطان الغدة الرئوية ، يمكن أن يؤثر بعضها على سرطان الخلايا الحرشفية بجعلها أكثر عدوانية.
يمكن تحديد طفرات EGFR في كل من الورم الأولي (الأصلي) وفي النقائل (الأورام الثانوية التي انتشرت إلى مواقع بعيدة). تميل هذه الطفرات إلى التحور السريع وغالبًا ما تصبح مقاومة للأدوية المستخدمة في علاجها.
كراس
إن جين KRAS مسؤول عن إنتاج بروتين إشارة يسمى K-Ras الذي يوجه الخلايا حول كيفية الانقسام والنضج والوظيفة. يمكن أن يؤدي عدم تنظيم هذا البروتين إلى الإصابة بالسرطان.
ما يقرب من 15 ٪ إلى 20 ٪ من الأشخاص المصابين بالسرطان الغدي في الرئة إيجابية لطفرات KRAS. تحدث هذه غالبًا جنبًا إلى جنب مع طفرات EGFR.
يتم تحديد طفرات KRAS بشكل أساسي في الورم الأولي وأقل شيوعًا في الأورام النقيلية.
ALK
جيناز سرطان الغدد الليمفاوية الكشمي (ALK) مسؤول عن إنتاج نوع من بروتين التيروزين كيناز الذي يوجه الخلايا للانقسام والنمو. الطفرة ، التي يشار إليها بشكل أكثر دقة باسم إعادة ترتيب ALK ، مرتبطة بـ NSCLC وهي أكثر شيوعًا في الآسيويين من أي مجموعة أخرى.
ترتبط إعادة ترتيب ALK بنسبة تتراوح بين 3٪ و 5٪ من حالات NSCLC (السرطانات الغدية بشكل أساسي) وهي أكثر شيوعًا عند المدخنين الخفيفين وغير المدخنين والأشخاص الذين تقل أعمارهم عن 70 عامًا.
BRCA2
لقد وجد أن الأشخاص الذين يعانون من طفرة جينية BRCA2 ، وهي إحدى الطفرات المرتبطة بسرطان الثدي ، هم أكثر عرضة للإصابة بسرطان الرئة أيضًا.
تم العثور على هذه الطفرة في ما يقرب من 2 ٪ من الأشخاص من أصل أوروبي وهي موروثة في نمط جسمي سائد (بمعنى أن أحد الوالدين فقط يجب أن يساهم في الطفرة لزيادة خطر الإصابة بمرض).
المدخنون الذين لديهم طفرة في BRCA2 هم أكثر عرضة للإصابة بسرطان الرئة مرتين تقريبًا من عامة السكان. على النقيض من ذلك ، فإن غير المدخنين المصابين بطفرة BRCA لديهم مخاطر متزايدة بشكل طفيف.
غالبًا ما يصاب المدخنون الذين يحملون هذه الطفرة بسرطان الخلايا الحرشفية. تتطور سرطانات الخلايا الحرشفية في الممرات الهوائية للرئتين ، على عكس الأورام الغدية التي تتطور على الحواف الخارجية للرئتين.
الفحص والعلاج
لا يزال لدى العلماء الكثير لتعلمه عن علم الوراثة لسرطان الرئة. على الرغم من وجود ارتباطات واضحة بين سرطان الرئة وطفرات EGFR و KRAS و ALK و BRAF ، يُعتقد أن هذه الطفرات مكتسبة ولا توجد إلا في الخلايا السرطانية وليس في خلايا الجسم الأخرى. لذلك لا يمكن التعرف عليها قبل الإصابة بسرطان الرئة (ولكن يمكن تحديد بعض الطفرات الموروثة مثل BRCA1 و BRCA2 مسبقًا).
في الوقت الحالي ، لا توجد توصيات بشأن الفحص الجيني لسرطان الرئة. لا تزال التحقيقات البحثية التي تهدف إلى تحديد الجينات الموروثة التي تؤدي إلى الإصابة بسرطان الرئة أو تهيئ لها لا تقدم معلومات نهائية.
حيث يمكن أن تساعد الاختبارات الجينية في اختيار العلاجات المستهدفة لعلاج سرطان الرئة. باستخدام هذا النوع من النهج ، يتم اختبار أنسجة سرطان الرئة بحثًا عن الطفرات الجينية ، ويمكن استخدام علاج السرطان الذي يقضي على الخلايا السرطانية على وجه التحديد التي تحتوي على الطفرة الجينية المحددة.
تستهدف هذه الأدوية الخلايا السرطانية بطفرات معينة قابلة للعلاج وتقتلها ، تاركة الخلايا الطبيعية سليمة إلى حد كبير. لهذا السبب ، غالبًا ما تسبب العلاجات المستهدفة آثارًا جانبية أقل.
من بين الأدوية المستهدفة المستخدمة في NSCLC مع طفرة EGFR:
- جلوتريف (أفاتينيب)
- إيريسا (جيفيتينيب)
- تاجريسو (أوسيمرتينيب)
- تارسيفا (إرلوتينيب)
- Vizimpro (داكوميتينيب)
من بين الأدوية المستهدفة المستخدمة في NSCLC مع إعادة ترتيب ALK:
- أليسينسا (ألكتينيب)
- ألونبريج (بريجاتينيب)
- لوربرينا (لورلاتينيب)
- Xalkori (كريزوتينيب)
- زيكاديا (سيريتينيب)
كلمة من Verywell
إذا كنت معرضًا لخطر كبير للإصابة بالمرض ، فقد تستفيد من الفحص السنوي بالأشعة المقطعية لسرطان الرئة. يوصى بالفحص السنوي حاليًا للأشخاص الذين تتراوح أعمارهم بين 50 و 80 عامًا ممن يدخنون أو أقلعوا عن التدخين خلال الـ 15 عامًا الماضية ولديهم تاريخ تدخين 20 عبوة على الأقل.
اعتمادًا على عوامل الخطر الإضافية ، مثل تاريخ العائلة أو التعرض للرادون ، قد تختار أنت وطبيبك الفحص خارج هذه المعايير. قد يؤدي القيام بذلك إلى الإصابة بسرطان الرئة مبكرًا بينما لا يزال قابلاً للعلاج بشكل كبير.












.jpg)