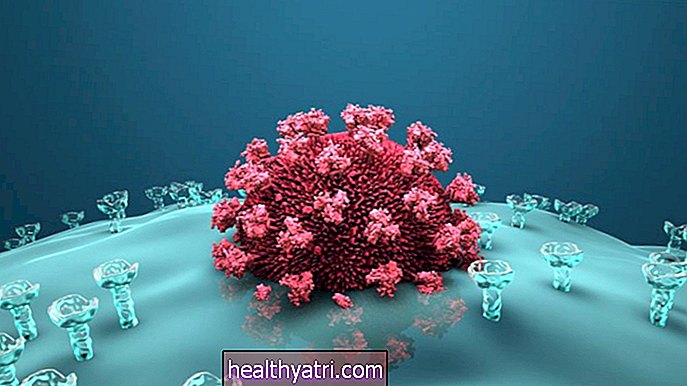
يستخدم العلاج المضاد للفيروسات القهقرية لعلاج فيروس نقص المناعة البشرية ويتألف من مجموعة من الأدوية التي تمنع المراحل المختلفة في دورة تكاثر الفيروس. من خلال القيام بذلك ، يمكن قمع الفيروس إلى مستويات لا يمكن اكتشافها حيث يمكن أن يتسبب في ضرر ضئيل للجسم.
تم الإبلاغ عن فعالية الجمع بين العلاج المضاد للفيروسات القهقرية لأول مرة من قبل الباحثين في عام 1996 في مؤتمر الإيدز الدولي في فانكوفر ، الذين أطلقوا على نهج HAART (العلاج بمضادات الفيروسات القهقرية النشطة للغاية).
جاستن سوليفان / غيتي إيماجز نيوز / جيتي إيماجيساليوم ، مصطلح HAART أقل استخدامًا وقد تم استبداله إلى حد كبير في الأدبيات الطبية بواسطة ART المبسط (العلاج المضاد للفيروسات القهقرية). التغيير في المصطلحات يدور حول أكثر من مجرد دلالات. إنه يعكس تحولًا في أهداف وفوائد علاج فيروس نقص المناعة البشرية وخطوة بعيدًا عما أشارت إليه HAART تاريخيًا.
قبل HAART
عندما تم التعرف على أولى حالات الإصابة بفيروس نقص المناعة البشرية في الولايات المتحدة في عام 1982 ، سارع العلماء إلى إيجاد طرق لعلاج فيروس ليس له أسبقية تذكر في الطب الحديث.
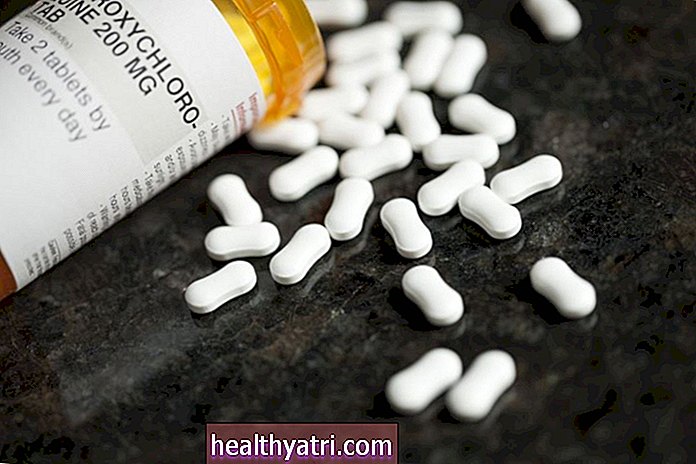
سوف يستغرق الأمر خمس سنوات قبل أن تتم الموافقة على أول دواء مضاد للفيروسات القهقرية ، يسمى AZT (زيدوفودين) ، من قبل إدارة الغذاء والدواء الأمريكية (FDA) في مارس من عام 1987. وقد قدم للجمهور أول تأكيد بأن المرض ، الذي يعتبر إلى حد كبير عقوبة الإعدام ، يمكن السيطرة عليها في يوم من الأيام.
على الرغم من الاختراق المبكر ، قدم AZT فقط فوائد متواضعة ، مما زاد من أوقات البقاء على قيد الحياة بمعدل 24 شهرًا.
أدى التطور السريع لمقاومة الأدوية إلى زيادة استخدام الدواء ، في حين أن التأثيرات السامة للعقار غالبًا ما تركت المستخدمين يعانون من فقر الدم الحاد ، ومشاكل في الكبد ، ومضاعفات أخرى لا تطاق.
بحلول عام 1988 ، تمت الموافقة على ثلاثة عقاقير أخرى بسرعة - Hivid (ddC ، zalcitabine) ، Videx (ddI ، ديدانوزين) ، و Zerit (d4T ، ستافودين) - واستخدمت في العلاجات المركبة في محاولة لإطالة متوسط العمر المتوقع. وعلى الرغم من أنها ساعدت بالتأكيد ، إلا أنها أثبتت أنها أكثر سمية من عقار AZT وتطلبت جداول جرعات معقدة ، غالبًا مع جرعات متعددة تؤخذ على مدار النهار والليل.
ما بدأ الباحثون يدركون بسرعة هو أن هذه الأدوية - والأدوية اللاحقة مثل Viramune (nevirapine) و Epivir (3TC ، lamivudine) - فشلت في تحقيق السيطرة الدائمة لأن لديهم جميعًا آليات عمل متشابهة وأعاقت فقط واحدة من المراحل السبع من العلاج. دورة تكاثر الفيروس.
تم اقتراح أنه من خلال استهداف المراحل الأخرى ، سيكون للفيروس فرصة أقل للتكاثر ويمكن السيطرة عليه بالكامل. بدأ تحقيق هذا الوعد في عام 1995 بإدخال فئة جديدة من الأدوية المضادة للفيروسات القهقرية تعرف باسم مثبطات الأنزيم البروتيني (PIs).
ظهور HAART
في عام 1995 ، وافقت إدارة الغذاء والدواء الأمريكية على أول مثبط للبروتياز يسمى Invirase (saquinavir). على عكس مضادات الفيروسات القهقرية الأخرى في ذلك الوقت ، والتي أعاقت قدرة الفيروس على "اختطاف" الآلية الوراثية للخلية وتحويلها إلى مصنع لإنتاج فيروس نقص المناعة البشرية. منع قدرة الفيروس على تجميع نسخ جديدة من نفسه من البروتينات الهيكلية.
أثبت هذا النهج الثنائي أنه نقطة التحول في الوباء المتنامي.
تم الإبلاغ في مؤتمر 1996 في فانكوفر أن الاستخدام الاستراتيجي لثلاثة عقاقير من كل من الفئتين كان قادرًا على تحقيق واستدامة حمولة فيروسية غير قابلة للاكتشاف ، مما أدى إلى تعافي المرض بشكل فعال.
تمت تسمية النهج الجديد بسرعة HAART وتم تنفيذه على الفور كمعيار للرعاية. في غضون ثلاث سنوات قصيرة ، تراجعت وفيات فيروس نقص المناعة البشرية في الولايات المتحدة وأوروبا بنسبة تزيد عن 50٪ - وهو أول تراجع من نوعه منذ بداية الوباء.
ومع ذلك ، كان HAART بعيدًا عن الكمال ، وكان متوسط العمر المتوقع ، على الرغم من تحسنه بشكل كبير ، أقل من متوسط العمر المتوقع لعامة السكان. بحلول نهاية القرن ، من المحتمل أن يعيش شاب يبلغ من العمر 20 عامًا يخضع للعلاج بمضادات الفيروسات العكوسة حتى أوائل الخمسينيات من عمره.
في هذا السياق ، كان "فعال للغاية" مؤشرا على قيود HAART مثل فوائده.
ما وراء HAART
بحلول عام 2000 ، أصبحت القيود المفروضة على العقاقير المضادة للفيروسات العكوسة المتاحة واضحة للعيان. على الرغم من قدرتها على تحقيق كبت الفيروس ، إلا أنها قد تمثل تحديًا كبيرًا للمستخدم لعدة أسباب مختلفة:
- ارتبطت مثبطات البروتياز في ذلك الوقت بتأثيرات استقلابية شديدة محتملة ، بما في ذلك الحثل الشحمي (إعادة توزيع دهون الجسم المشوهة أحيانًا) ، ومقاومة الأنسولين ، وعدم انتظام ضربات القلب.
- يمكن أن تسبب AZT و Zerit والأدوية الأخرى المصنفة على أنها مثبطات النسخ العكسي للنيوكليوزيد (NRTIs) اعتلالًا عصبيًا طرفيًا شديدًا وحماض لبنيًا قد يهدد الحياة.
- كانت الأدوية في ذلك الوقت أقل "تسامحًا" وتخضع للتطور السريع لمقاومة الأدوية إذا كان الالتزام بالعلاج أقل من الكمال. بعض مثبطات النسخ العكسي غير النوكليوزيدية (NNRTIs) مثل Viramune يمكن أن تطور مقاومة مع طفرة فيروسية واحدة .
- تتطلب بعض مثبطات البروتياز ، مثل Invirase ، ثلاث كبسولات كل 8 ساعات - وهو جدول وجد الكثير من الصعب الحفاظ عليه على المدى الطويل.
كانت هذه المشكلات إشكالية للغاية لدرجة أن HAART تأخر بشكل قياسي حتى انخفضت وظيفة المناعة إلى ما دون عتبة معينة (أي عدد CD4 أقل من 350). لوحظ أن مخاطر العلاج المبكر في ذلك الوقت تفوق الفوائد.
تغير كل ذلك في عام 2001 مع إدخال Viread (tenofovir disoproxil fumarate) ، وهو نوع جديد من NRTI كان له آثار جانبية أقل بكثير ، ويمكن أن يتغلب على المقاومة العميقة ، ويتطلب حبة واحدة فقط يوميًا.
بحلول عام 2005 ، مع زيادة معدلات العمر المتوقع وانخفاض معدلات الوفيات في جميع أنحاء العالم ، تمكن الباحثون من إثبات أن علاج فيروس نقص المناعة البشرية في وقت التشخيص منع الإصابة الشديدة بفيروس نقص المناعة البشرية وغير المرتبط بفيروس نقص المناعة البشرية. الأمراض بنسبة مذهلة بلغت 61٪.
مع العلاج الشامل للتشخيص أصبح المعيار الجديد في جميع أنحاء العالم ، بدأ المجتمع الطبي في استخدام ART لوصف نهج علاجي أصبح الآن أكثر من مجرد "فعال للغاية".
ART اليوم
يتمثل الاختلاف الرئيسي بين العلاج عالي التأثير المضاد للفيروسات القهقرية في أواخر التسعينيات / أوائل القرن الحادي والعشرين و ART اليوم في أنه يمكن اعتبار فيروس نقص المناعة البشرية حقًا حالة مزمنة يمكن التحكم فيها. لا يمكن فقط لشخص يبلغ من العمر 20 عامًا تم تشخيص إصابته بفيروس نقص المناعة البشرية اليوم أن يعيش جيدًا في السبعينيات من عمره ، ولكن يمكنه فعل ذلك بأدوية أكثر أمانًا وطويلة الأمد وأسهل في تناولها.
فئات الأدوية والعقاقير الأحدث
في السنوات الأخيرة ، تم تطوير فئات جديدة من الأدوية المضادة للفيروسات القهقرية لمهاجمة الفيروس بطرق مختلفة. يمنع البعض ارتباط فيروس نقص المناعة البشرية بالخلايا المضيفة (مثبطات الدخول / التعلق) ، بينما يمنع البعض الآخر تكامل الترميز الفيروسي في نواة الخلية المضيفة (مثبطات الإنزيم).
بالإضافة إلى ذلك ، تم إنشاء إصدارات أحدث من PIs و NRTIs و NNRTIs التي توفر حركية دوائية أفضل (نشاط دوائي) وآثار جانبية أقل وملامح أفضل لمقاومة الأدوية.
أحد الأمثلة على ذلك هو نسخة محدثة من Viread تسمى tenofovir alafenamide (TAF). بدلاً من توصيل الدواء مباشرة ، فإن TAF هو "عقار أولي" غير نشط يتم تحويله بواسطة الجسم إلى تينوفوفير. يؤدي هذا إلى خفض الجرعة من 300 مجم إلى 25 مجم مع نفس النتائج السريرية مع تقليل مخاطر الإصابة بمشاكل الكلى المرتبطة باستخدام Viread.
الأدوية المركبة بجرعات ثابتة
تقدم آخر في العلاج هو تطوير الأدوية المركبة بجرعة ثابتة (FDC) التي يمكن أن تقدم علاجًا كاملاً بحبوب واحدة فقط يوميًا. اليوم ، هناك 13 من هذه الأدوية الكل في واحد تمت الموافقة عليها من قبل إدارة الغذاء والدواء.
لم تُحسِّن تركيبات الحبوب المفردة معدلات الالتزام فحسب ، بل ثبت أنها تقلل بشكل كبير من خطر الإصابة بالأمراض الشديدة والاستشفاء مقارنةً بالعلاجات المضادة للفيروسات العكوسة.
إعادة تعريف العلاج المركب
لطالما كان مصطلح HAART مرادفًا للعلاج بالعقاقير الثلاثية. وفي حين أنه من الصحيح أن العلاج المضاد للفيروسات القهقرية يتكون عادة من ثلاثة أو أكثر من مضادات الفيروسات القهقرية ، فإن الحرائك الدوائية المحسنة جعلت من الممكن الآن علاج فيروس نقص المناعة البشرية باستخدام اثنين فقط من الأدوية المضادة للفيروسات القهقرية.
في عام 2019 ، وافقت إدارة الأغذية والعقاقير (FDA) على أول علاج كامل من دوائين يُعرف باسم Dovato ، والذي يجمع بين جيل جديد من مثبطات Integrase يسمى dolutegravir وهو NRTI أقدم يسمى lamivudine. لقد أثبت هذا المزيج فعاليته مثل العلاج الثلاثي القياسي مع آثار جانبية أقل.
كما تحول تعريف العلاج بمضادات الفيروسات القهقرية على أذنه إلى إطلاق علاج عام 2021 عن طريق الحقن يُعرف باسم كابينوفا.
كابينوفا هو الأولمرة كل شهرالعلاج قادر على تحقيق قمع فيروسي مستدام بحقنة واحدة من مثبطات إنزيم إنجراز كابوتغرافير وحقنة واحدة من NNRTI أحدث يسمى rilpivirine.
مثل هذه التطورات تعيد تعريف معنى ART وما يمكن أن تصبح عليه في النهاية.
كلمة من Verywell
على الرغم من أن أهداف العلاج المضاد للفيروسات القهقرية لا تزال كما هي ، فإن العلاج المضاد للفيروسات القهقرية اليوم لا يحمل سوى تشابه سريع مع HAART في الماضي. بدون استثناء ، تفوق فوائد العلاج بكثير أي مخاوف قد تكون لديك بشأن الأدوية أو آثارها الجانبية.
علاوة على ذلك ، تمتد الفوائد إلى أولئك غير المصابين. نُشر بحث بارز في إصدار 2019 مناللانسيتخلص إلى أن الأشخاص المصابين بفيروس نقص المناعة البشرية الذين يصابون بفيروس لا يمكن اكتشافه لديهم فرصة معدومة لإصابة الآخرين.
توضح هذه العوامل أيضًا الحاجة إلى اختبار فيروس نقص المناعة البشرية وتوضح سبب توصية فريق عمل الخدمات الوقائية بالولايات المتحدة بإجراء اختبار فيروس نقص المناعة البشرية لمرة واحدة لجميع الأمريكيين الذين تتراوح أعمارهم بين 15 و 65 عامًا كجزء من زيارة الطبيب الروتينية.


.jpg)
.jpg)















-and-sunscreen.jpg)
