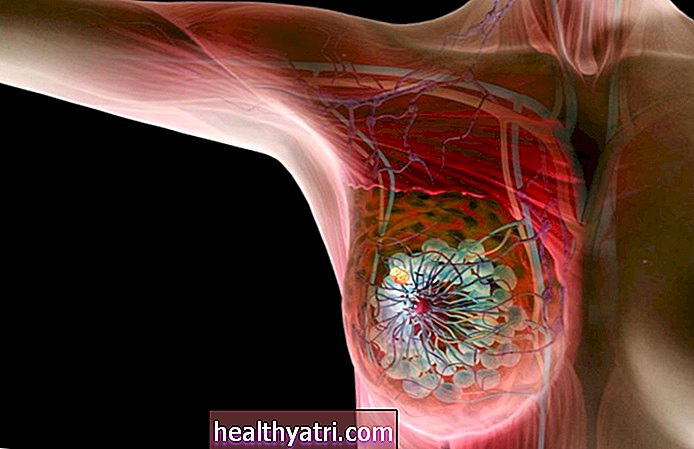
يشير العلاج اللاإرادي للورم إلى علاجات السرطان التي تعمل عبر أنواع السرطان. بمعنى آخر ، بدلاً من العمل مع نوع واحد فقط من السرطان ، مثل سرطان الثدي ، قد تعمل هذه العلاجات مع عدد من أنواع السرطان المختلفة ، على سبيل المثال ، الورم الميلانيني وسرطان الثدي والساركوما. بالإضافة إلى ذلك ، يمكنهم العمل لكل من البالغين والأطفال.
Panuwat Dangsungnoon / iStock
بدلاً من العلاجات القائمة على المكان الذي نشأ فيه الورم ، يعالج هذا العلاج السرطان الذي ينشأ في أي مكان بناءً على الخصائص الجزيئية المعينة التي تدفع نمو الورم. على الرغم من ظهورها في أنسجة مختلفة ، فليس من غير المألوف أن تستخدم أنواع مختلفة جدًا من السرطان نفس المسار للنمو
إن الفهم المتزايد لبيولوجيا السرطان ، والقدرة على إجراء الاختبارات الجينية لتحديد ما يدفع نمو سرطان معين ، وتوافر الأدوية التي تستهدف هذه المسارات قد أعطت الباحثين القدرة على علاج مجموعة واسعة من السرطانات على المستوى الجزيئي .
لا يوجد حاليًا سوى عدد قليل من الأدوية المعتمدة خصيصًا للعلاج اللاإرادي للورم ولكن من المتوقع أن يتوسع هذا بسرعة في المستقبل القريب جدًا. سنلقي نظرة على تعريف وأهمية العلاجات اللاإرادية للورم ، والأمثلة التي يتم استخدامها حاليًا ، وفوائد وقيود نهج العلاج هذا.
تعريف العلاج اللاأشاري للورم
يشير العلاج اللاأدري للورم إلى استخدام الأدوية لعلاج السرطان بناءً على التركيب الجزيئي للورم بدلاً من الموقع الأصلي للسرطان.
أهمية
تطورت علاجات السرطان بحيث يتم بالفعل اختيار علاجات لأنواع معينة من السرطان (مثل سرطان الرئة) بناءً على الخصائص الجزيئية للورم.
على سبيل المثال ، مع سرطان الرئة ذو الخلايا غير الصغيرة ، بدلاً من اختيار العلاجات التي تعتمد أساسًا على ما يظهر تحت المجهر ، فإن الاختبارات الجينية (مثل تسلسل الجيل التالي) تسمح للأطباء بتحديد ما إذا كان السرطان يحتوي على طفرة جينية معينة (أو أي تغيير آخر ) التي تتوفر لها العلاجات المستهدفة الآن.
بينما يمكن إعطاء دواء معين للعلاج الكيميائي لأكثر من نوع واحد من السرطان ، فإن المبدأ الكامن وراء العلاج مختلف. يعالج العلاج الكيميائي بشكل أساسي أي خلايا تنقسم بسرعة.
في المقابل ، تستهدف العلاجات المستهدفة (وبطريقة مختلفة ، أدوية العلاج المناعي) مسارًا محددًا جدًا في النمو. قد يستجيب نوعان من السرطانات من نفس النوع والمرحلة ويستجيبان بشكل مشابه للعلاج الكيميائي بشكل مختلف تمامًا للعلاج بالعقار المستهدف.
إذا كان الورم يحتوي على طفرة ، مثل طفرة EGFR ، فإن استخدام دواء يستهدف الطفرة (مثل مثبط EGFR) من المحتمل جدًا أن يؤدي إلى التحكم في نمو السرطان. في المقابل ، إذا كان الورم الذي لا يحتوي على هذه الطفرة فمن غير المرجح أن يستجيب على الإطلاق لمثبط EGFR.
العلاجات التي تستهدف هذه التعديلات الجينومية المحددة (والتي يشار إليها أحيانًا باسم "التوقيع الجزيئي" للورم) قد غيرت بشكل كبير علاج العديد من أنواع السرطان ، وكذلك التركيز على تطوير الأدوية.
علم الأحياء والمصطلحات
من أجل مناقشة العلاجات المحايدة للورم ، من المفيد التحدث عن بعض البيولوجيا المربكة. لحسن الحظ ، أصبح الناس أكثر قوة ويتعلمون عن سرطاناتهم ، لكن الأمر لا يختلف عن تعلم لغة أجنبية صعبة.
لكي يستمر السرطان في النمو ، يجب أن تكون الخلايا مختلفة بما يكفي عن الخلايا الطبيعية بحيث لا تستمع إلى إشارات الجسم الطبيعية للتوقف عن النمو أو القضاء على نفسها. هناك مسارات معقدة تشارك في نمو الخلايا ، ويمكن أن تؤدي التشوهات في عدد من هذه النقاط إلى نمو غير متحكم فيه.
الطفرات الجينية (والتغيرات الأخرى) هي أساس السرطان ، وهي سلسلة من هذه الطفرات التي تؤدي إلى تحول الخلية إلى خلية سرطانية. الجينات هي مخطط البروتينات ، والبروتينات بدورها هي العوامل التي إما تحفز أو تثبط النقاط المختلفة على هذه المسارات.
يوجد الآن عدد من الأدوية (والعديد منها قيد التطوير والتجارب السريرية) التي تمنع بعض هذه البروتينات ، وبالتالي توقف الإشارات التي تؤدي إلى استمرار نمو السرطان. بعض المصطلحات تبدو محيرة للغاية ولكنها واضحة إلى حد ما عند تعريفها.
يشير مصطلح الطفرة الدافعة إلى طفرة في جين يرمز لبروتين يتحكم في نمو السرطان. السرطانات التي تحتوي على هذه الطفرة (أو أي تغيير آخر) "تعتمد" على البروتين غير الطبيعي المنتج لمواصلة النمو. غالبًا ما يستخدم أطباء الأورام مصطلح إدمان الجينات الورمية لوصف هذا السلوك.
عندئذٍ يُطلق على الطفرة الخاصة اسم التوقيع الجزيئي للسرطان.
معايير العلاجات اللاأشرافية للورم
من أجل أن يكون العلاج فعالًا عبر أنواع السرطان ، هناك عدد قليل من المعايير التي يتم استخدامها.
- يجب العثور على الطفرة المعينة (أو أي تغيير آخر). بمعنى آخر ، يجب أن يكون الاختبار متاحًا لاكتشاف التغيير وأن يتم إجراؤه كثيرًا.
- يجب أن تستجيب الأورام التي تحتوي على طفرة معينة للعلاجات التي تستهدف العلاج.
- يجب العثور على الطفرة في العديد من أنواع السرطان المختلفة.
الاستخدامات والأمثلة
يوجد حاليًا عدد قليل من الأدوية التي تمت الموافقة عليها للاستخدام المحايد للورم وأخرى يتم استخدامها خارج التسمية بهذه الطريقة. سننظر في بعض هذه الأدوية.
كيترودا
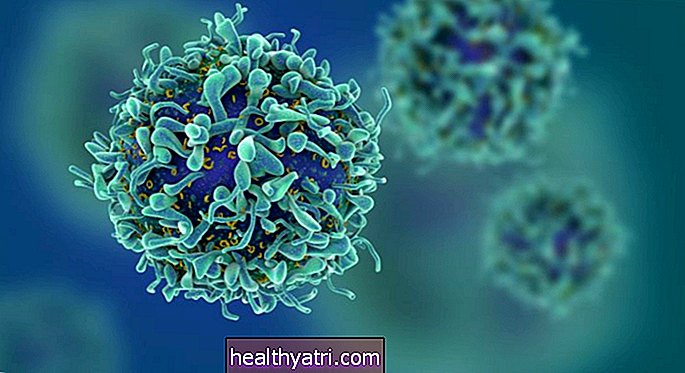
كان Keytruda (pembrolizumab) أول دواء تمت الموافقة عليه لعلاج الورم اللاإرادي في عام 2017. Ketruda هو جسم مضاد أحادي النسيلة PD-a مصنف على أنه نقطة تفتيش inhitibor (نوع من أدوية العلاج المناعي). وهو يعمل بشكل أساسي عن طريق "إزالة الفرامل" استجابة الجهاز المناعي للجسم للسرطان.
تمت الموافقة على Keytruda للأورام الصلبة لدى البالغين أو الأطفال الذين تم العثور على عدم استقرار عالٍ في السواتل المكروية (MSI-H) أو يعانون من نقص في إصلاح عدم التطابق (dMMR). يمكن العثور على MSI-H أو dMMR من خلال الاختبارات التي يتم إجراؤها على الورم (تفاعل البوليميراز المتسلسل أو الكيمياء النسيجية المناعية).
في عام 2020 ، حصل Keytruda على موافقة ثانية على عدم تشخيص الورم للأشخاص الذين يعانون من أورام صلبة تحمل عبئًا تحورًا كبيرًا. عبء الطفرة هو مقياس لعدد الطفرات الموجودة في الورم السرطاني ، ويرتبط (ولكن ليس دائمًا) بالاستجابة الإيجابية لأدوية العلاج المناعي.
فيتراكفي
Vitrakvi (larotrectinib) هو الدواء الثاني الذي حصل على الموافقة على العلاج اللاإرادي للورم في عام 2018. وقد تمت الموافقة عليه للبالغين أو الأطفال المصابين بأورام ببروتينات الاندماج NTRK. تم العثور على اندماج جيناز مستقبلات التغذية العصبية (NTRK) في حوالي 1 ٪ فقط للعديد من الأورام الصلبة ، مثل سرطان الرئة ، ولكنها قد تكون موجودة في ما يصل إلى 60٪ من بعض أنواع الأورام اللحمية.
بعض أنواع السرطانات التي تم إثبات الاستجابة لها تشمل سرطان الرئة ، سرطان الجلد ، أورام الجهاز الهضمي ، سرطان القولون ، أورام الأنسجة الرخوة ، أورام الغدد اللعابية ، الساركوما الليفية الطفولية ، سرطان الثدي ، وسرطان البنكرياس.
في البالغين المصابين بأورام تحوي اندماج الجين NTRK ، كان معدل الاستجابة لفيتراكفي 75٪ إلى 80٪ ، وفي تجربة منفصلة للأطفال ، كان معدل الاستجابة الإجمالي 90٪.
شوهدت هذه الاستجابات حتى عندما تلقى الأشخاص علاجات سابقة. ما يفعله هذا هو تأكيد مدى اعتماد هذه الأورام على هذا المسار للنمو. لم تكن الردود عالية فحسب ، بل إن استخدام Vitrakvi كان قادرًا على كسب بعض الحالات والسماح للجراحين بإجراء عمليات جراحية أقل تشوهًا للأطفال.
روزليتريك
في عام 2019 ، وافقت إدارة الغذاء والدواء الأمريكية على استخدام Rozlytrek (entrectinib) للأشخاص المصابين بأورام تؤوي اندماج الجينات NTRK وكذلك لسرطان الرئة ذو الخلايا غير الصغيرة مع تغيير ROS1.
تمت الموافقة على الدواء للبالغين أو الأطفال المصابين بالسرطان النقيلي أو الذين يمكن أن تؤدي الجراحة إلى تشوه كبير. خلال التقييم ، كانت الاستجابة الإجمالية نادرة 78٪.
وكانت السرطانات الأكثر شيوعًا في الدراسة هي الساركوما ، وسرطان الرئة ذو الخلايا غير الصغيرة ، وسرطان الثدي ، وسرطان القولون والمستقيم ، وسرطان الغدة الدرقية ، وسرطان الثدي التماثلية.
طفرات BRAF
على الرغم من عدم الموافقة على علاج محدد للورم ، فقد وجد الباحثون أن الأشخاص الذين يعانون من أنواع مختلفة من السرطانات التي تحتوي على طفرات BRAF غالبًا ما يستجيبون للعلاج بمثبطات BRAF (عادةً بالاشتراك مع مثبطات MEK).
لوحظت طفرات BRAF في البداية (وعولجت) في الأشخاص المصابين بسرطان الجلد النقيلي ، ولكن تم إثباتها الآن في سرطان الرئة ذو الخلايا غير الصغيرة (حوالي 3٪) ، وسرطان القولون ، وسرطان الدم مشعر الخلايا ، وسرطان الغدة الدرقية ، وسرطان المبيض المصلي ، وغيرها.
أمثلة أخرى
نظرًا لإجراء اختبارات الجيل التالي في كثير من الأحيان ، بدأ الباحثون في رؤية التغيرات الجينية التي كان يُعتقد أنها معزولة عن نوع واحد من السرطان في أنواع أخرى.
على سبيل المثال ، التغيير الملحوظ مع سرطان الثدي الإيجابي HER2 موجود لدى بعض الأشخاص المصابين بسرطان الرئة.تشمل الأمثلة الأخرى استخدام عقار Lynparza (olaparib) ليس فقط لسرطان الثدي ، ولكن أيضًا لسرطان المبيض وسرطان البروستاتا وسرطان البنكرياس الذي يؤوي طفرة BRCA.
الاختبار والمحاكمات
هناك عدد من الأدوية قيد التطوير بالإضافة إلى الأدوية الخاضعة للتجارب السريرية في هذا الوقت. تشمل أنواع التجارب السريرية التي تقيِّم أحيانًا الأدوية عبر فئات مختلفة من السرطان التجارب الشاملة والتجارب الشاملة. يتم تسهيل التقييم من خلال بروتوكول مطابقة دقيقة يسمى NCI-MATCH.
الفوائد والقيود
هناك فوائد واضحة عندما يتعلق الأمر بالقدرة على استخدام علاج واحد لعدة أنواع مختلفة من السرطان ، ولكن هناك أيضًا قيود.
فوائد
وغني عن القول أن الأدوية اللاأدريّة للورم لها فوائد عندما يتعلق الأمر بالبحث عن الأدوية وتطويرها. تطوير الأدوية مكلف للغاية. لكن المكان الذي يبرز فيه هذا النهج حقًا هو علاج السرطانات النادرة.
مع السرطانات التي تصيب نسبة صغيرة فقط من السكان (على سبيل المثال ، الساركوما الليفية عند الأطفال) ، لا "تدفع" الشركة بالضرورة لدراسة الأدوية وتطويرها. هذا لا يعني أن الأمر ليس مهمًا ، لكن الشركات تميل إلى استثمار الأموال بطرق تجعلها ترى عائدًا.
ومع ذلك ، مع العلاجات اللاإرادية للأورام ، قد تتلقى شركات الأدوية تعويضات عندما يكون هناك عدد من الأشخاص المصابين بأنواع السرطان الأكثر شيوعًا والذين يستفيدون من الدواء. مثال على ذلك هو فيتراكفي.
فائدة أخرى قوية هي أن البحث يعمل على تطوير العلم المحيط بالسرطان. لكن دراسة المسارات الجزيئية للنمو على أمل العثور على علاج ، يتم اكتشاف مسارات جديدة بأمل لمزيد من العلاجات.
القيود / المخاطر
في حين أن العلاجات اللاأدرازية للورم قد تبدو كهدف علاجي في المستقبل ، إلا أن هناك عددًا من القيود على استخدامها.
ليست كل السرطانات تستجيب بنفس الطريقة
حتى عندما يكون لنوعين مختلفين من السرطان نفس الطفرة التي تحرك نمو السرطان ، فإن الاستجابة لعقار يستهدف تلك الطفرة قد تكون مختلفة تمامًا.
مثال على ذلك مع طفرات BRAF V600E. تميل الأورام الميلانينية أو خلايا ابيضاض الدم مشعر الخلايا التي تأوي الطفرة إلى أن تكون شديدة الاستجابة للأدوية التي تثبط BRAF. في المقابل ، لا تميل سرطانات القولون التي لها نفس الطفرة إلى الاستجابة لمثبطات BRAF.
قد يتطلب نوعان من السرطان لهما نفس الطفرة المحركة علاجات مختلفة جدًا للتحكم في النمو.
قيد آخر هو أن الاختبارات الجينومية لم تصبح روتينية بعد لجميع الأشخاص حتى المصابين بالسرطان الذي يوصى به بشدة (على سبيل المثال ، مع سرطان الرئة ذو الخلايا غير الصغيرة). مع بعض أنواع السرطانات ، خاصة تلك التي لا تظهر بشكل متكرر ، قد يكون هناك القليل من البيانات المتعلقة بالخصائص الجزيئية الشائعة الموجودة.
في أغلب الأحيان ، لا يتوفر استخدام الأدوية الأحدث ، وخاصة العلاجات اللاإرادية للورم إلا من خلال التجارب السريرية. لا يقتصر الأمر على أن المشاركة في التجارب السريرية منخفضة للغاية في الولايات المتحدة فحسب ، بل هناك تباينات كبيرة في المشاركة تجعل تقييم العلاجات عبر العمر والعرق والجنس أكثر صعوبة.
يستغرق التطوير وقتًا أيضًا. وفقًا لإحدى الدراسات ، فإن متوسط الوقت من اكتشاف الأدوية إلى الاختبار والموافقة عليها في الولايات المتحدة هو 15 عامًا. وحتى عندما تصل هذه العلاجات إلى مستويات متقدمة في التجارب السريرية ، فإنها قد تساعد فقط أقلية من الناس.
أخيرًا ، يتم تسعير معظم العلاجات الجديدة للسرطان الآن في نطاق غير مستدام.
كلمة من Verywell
علاج السرطانات على أساس الخصائص الجزيئية ليس بالأمر الجديد ، ولكن استخدام هذه العلاجات في العديد من أنواع السرطان يمكن اعتباره طبًا دقيقًا للستيرويدات.
في حين أن أصل السرطان (علم الأنسجة) سيظل مهمًا ، فإن البدء في تركيز العلاج على الخصائص الجزيئية (الجينوميات والتشوهات المناعية وما إلى ذلك) يعد بالنهوض بمجال علم الأورام بطرق قد تفاجئنا بقدر التطورات الحديثة في العلاج الموجه و العلاج المناعي.
في الوقت نفسه ، من المثير التفكير في أن العلاج اللاأدري للورم قد يؤدي إلى علاجات للسرطانات النادرة (خاصة عند الأطفال) لم تكن لتتحقق لولا ذلك.